pembahasan selanjutnya adalah

Pembahasan soal-soal Ujian Nasional SMA IPA bidang studi Kimia dengan materi pembahasan Struktur Atom yang meliputi konfigurasi elektron, nomor atom, dan harga bilangan kuantum.
Soal Struktur Atom UN 2009
A. [Ne] 3s1
B. [Ne] 4s1
C. [Ar] 3s1
D. [Ar] 4s1
E. [Ar] 4s2 3d3
Pembahasan
Modal dasar untuk menyelesaikan soal ini adalah menghafal nomor atom gas mulia.
2He 10Ne 18Ar 36Kr 54Xe 86Rn
Pada struktur atom Q, yang perlu diperhatikan hanya nomor atomnya, yaitu 11.
11Q : 1s2 2s2 2p6 3s1
: [Ne] 3s1
Jadi, konfigurasi elektron unsur Q adalah [Ne] 3s1 (A).
Soal Struktur Atom UN 2011
A. 1s2 2s2 2p6 3s2 3p2
B. 1s2 2s2 2p6 3s2 3p4
C. 1s2 2s2 2p6 3s2 3p6
D. 1s2 2s2 2p6 3s2 3p6 3d2
E. 1s2 2s2 2p6 3s2 3p2 3d2

Pembahasan
Saat melakukan konfigurasi elektron, yang perlu diperhatikan adalah nomor atomnya (16). Untuk konfigurasi elektron ion, jumlah dan jenis muatan juga harus diperhatikan.
X−2 : atom X menangkap 2 elektron (jumlah elektron bertambah 2)
16X−2 : 16 + 2 = 18
Nah, sekarang tinggal kita periksa, opsi jawaban yang mempunyai jumlah elektron 18.
A. 1s2 2s2 2p6 3s2 3p2 (14)
B. 1s2 2s2 2p6 3s2 3p4 (16)
C. 1s2 2s2 2p6 3s2 3p6 (18)
D. 1s2 2s2 2p6 3s2 3p6 3d2 (20)
E. 1s2 2s2 2p6 3s2 3p2 3d2 (16)
Jadi, konfigurasi elektron ion X−2 adalah opsi (C).
Soal Struktur Atom UN 2012

Nomor atom dari X adalah ….
A. 17
B. 18
C. 21
D. 26
E. 30
Pembahasan
Diagram orbital di atas dapat diartikan
X : [Ar] 4s2 4p1
Ar adalah unsur gas mulia yang bernomor atom 18 sehingga nomor atom X adalah
18 + 2 + 1 = 21
Jadi, nomor atom unsur X adalah 21 (C).
Soal Struktur Atom UN 2013
A. n = 3; l = 1; m = −1; s = +½
B. n = 3; l = 1; m = −1; s = −½
C. n = 3; l = 0; m = −1; s = +½
D. n = 4; l = 0; m = 0; s = +½
E. n = 4; l = 0; m = 0; s = −½
Pembahasan
Konfigurasi elektron untuk unsur Ca adalah
20Ca : [Ar] 4s2
Elektron terakhir terletak pada 4s2.
- 4 menyatakan kulit keempat (n = 4)
- s menyatakan subkulit s (l = 0)
Ingat! s, p, d, f (sepeda federal) masing-masing mempunyai nilai l = 0, 1, 2, 3.
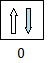
Di dalam subkulit s hanya terdapat satu ruang orbital yang diisi oleh 2 elektron.
- Elektron terakhir menempati orbital bernomor nol (m = 0)
- Elektron terakhir (biru) arahnya ke bawah (s = −½)
Jadi, harga keempat bilangan kuantum dari unsur Ca adalah n = 4; l = 0; m = 0; s = −½ (E).
Soal Struktur Atom UN 2015
A. n = 3; l = 0; m = −1; s = +½
B. n = 3; l = 0; m = +1; s = −½
C. n = 3; l = 1; m = +1; s = +½
D. n = 3; l = 2; m = 0; s = −½
E. n = 3; l = 1; m = 0; s = −½
Pembahasan
Konfigurasi atom Cl adalah
17Cl : [Ne] 3s2 3p5
Elektron terakhir terletak pada 3p5.
- Terletak pada kulit ke-3 (n = 3).
- Terletak pada subkulit p (l = 1)
Pada subkulit p terletak 3 ruang orbital yang berisi 5 elektron.
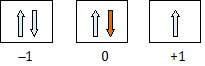
- Elektron terakhir (orange) menempati ruang 0 (m = 0)
- Elektron terakhir arahnya ke bawah (s = −½)
Jadi, harga keempat bilangan kuantum untuk elektron terakhir atom Cl adalah n = 3; l = 1; m = 0; s = −½ (E).
Pembahasan soal Struktur Atom yang lain bisa dibaca di:
Pembahasan Kimia UN 2014 No. 1
Pembahasan Kimia UN 2015 No. 4
Pembahasan Kimia UN 2016 No. 1
Pembahasan Kimia UN 2017 No. 3
Pembahasan Kimia UN 2018 No. 2
Pembahasan Kimia UN 2019 No. 2
Simak juga materi berikutnya, Pembahasan Kimia UN Sistem Periodik Unsur.
Dapatkan pembahasan soal dalam file pdf di sini.
Terimakasih
Semoga Bermanfaat