Untuk Pembelajaran selanjutnya…
Halo kali ini kita akan bahas mengenai tata nama senyawa biner. Senyawa biner merupakan senyawa yang dibentuk dari dua unsur. Agar lancar belajar kimia di tingkat berikutnya, maka wajib hukumnya tau tata nama senyawa. Kali ini kita mau bantu kamu dengan membuat rangkuman materi dan contoh soal tata nama senyawa biner. Jika ingin lebih paham kita buatkan juga video pembelajarannya disini. Selamat belajar
Tatanama Senyawa Ion
Senyawa Ion tersusun dari unsur logam (melepaskan elektron) dan non logam (menerima elektron). Unsur logam jika dibedakan berdasarkan berdasarkan jumlah biloksnya maka terbagi menjadi dua:
Senyawa Ion dengan logam memiliki jumlah satu biloks
Logam yang memiliki satu biloks pada umumnya adalah
- Golongan IA : Li, Na, K, Rb, Cs
- Golongan IIA : Be Mg, Ca, Sr, Ba
- Al, Zn dan beberapa logam lainnya
Tatanamanya:
Nama Logam + Nama Non Logam + akhiran -ida
Tatanama senyawa ion ini tidak menyebutkan biloks dan jumlah atomnya.
Contoh:
- NaBr = Natrium bromida
- K2O = Kalium oksida
- BaCl2 = Barium klorida
Senyawa Ion dengan logam memiliki jumlah biloks lebih dari satu
Logam yang memiliki lebih dari satu biloks pada umumnya adalah
- Golongan B (Transisi)
- Sn, Pb beberapa logam lainnya
Tatanamanya:
Nama Logam + (Biloks) + Nama Non Logam + akhiran -ida
Tatanama senyawa ion menyebutkan biloks, maka harus dihitung terlebih dahulu biloksnya. Tatanama senyawa ion ini juga tidak menyebutkan jumlah
Contoh:
Tuliskan nama Fe2O3
hitung terlebih dahulu biloks Fe
bo Fe x 2 + bo O x 3 = 0
2 b.o Fe + (-2) x 3 = 0
2 b.o Fe = +6
b.o Fe = +3
Maka namanya adalah Besi (III) Oksida
Tatanama Senyawa Kovalen
Senyawa kovalen tersusun dari unsur non logam (menerima elektron) dan non logam (menerima elektron).
Tata Namanya:
Jumlah NL 1 + Nama NL 1 + Jumlah NL 2 + Nama NL 2 + Akhiran
NL = Non Logam
Senyawa kovalen menuliskan jumlah unsurnya, kecuali pada unsur urutan pertama jika jumlahnya = 1 tidak disebutkan, nama jumlahnya yaitu:
- 1 = mono- (hanya disebut pada unsur urutan kedua)
- 2 = di-
- 3 = tri-
- 4 = tetra-
- 5 = penta-
- 6 = heksa-
- dst
Contoh :
- CO = Karbon monoksida
- CO2 = Karbon dioksida
- P2O5 = Diposfor pentaoksida
Tatanama Senyawa Kovalen
Senyawa kovalen tersusun dari unsur non logam (menerima elektron) dan non logam (menerima elektron).
Tata Namanya:
Jumlah NL 1 + Nama NL 1 + Jumlah NL 2 + Nama NL 2 + Akhiran
NL = Non Logam
Senyawa kovalen menuliskan jumlah unsurnya, kecuali pada unsur urutan pertama jika jumlahnya = 1 tidak disebutkan, nama jumlahnya yaitu:
- 1 = mono- (hanya disebut pada unsur urutan kedua)
- 2 = di-
- 3 = tri-
- 4 = tetra-
- 5 = penta-
- 6 = heksa-
- dst
Contoh :
- CO = Karbon monoksida
- CO2 = Karbon dioksida
- P2O5 = Diposfor pentaoksida
Tatanama Senyawa Poliatomik
Senyawa kovalen tersusun dari beberapa unsur lebih dari dua unsur. senyawa ini biasanya terdiri dari kation (ion positif) dan anion (ion negatif).
Tata Namanya:
Kation + Anion
Daftar Kation
|
No. |
Rumus Kation |
Nama Kation |
|
1. |
Li+ |
Litium |
|
2. |
Na+ |
Natrium |
|
3. |
K+ |
Kalium |
|
4. |
Rb+ |
Rubidium |
|
5. |
Cs+ |
Cesium |
|
6. |
Be2+ |
Berilium |
|
7. |
Mg2+ |
Magnesium |
|
8. |
Ca2+ |
Kalsium |
|
9. |
Sr2+ |
Stronsium |
|
10. |
Ba2+ |
Barium |
|
11. |
Fe2+ |
Besi (II) |
|
12. |
Fe3+ |
Besi (III) |
|
13. |
Cu+ |
Tembaga (I) |
|
14. |
Cu2+ |
Tembaga (II) |
|
15. |
Hg+ |
Raksa (I) |
|
16. |
Hg2+ |
Raksa (II) |
|
17. |
Ag+ |
Perak |
|
18. |
Au+ |
Emas (I) |
|
19. |
Au3+ |
Emas (III) |
|
20. |
Ni2+ |
Nikel |
|
21. |
Sn2+ |
Timah (II) |
|
22. |
Sn4+ |
Timah (IV) |
|
23. |
Ti2+ |
Titanium |
|
24. |
V2+ |
Vanadium |
|
25. |
Zn2+ |
Seng |
|
26. |
Co2+ |
Kobalt |
|
27. |
Al3+ |
Alumunium |
|
28. |
Pb2+ |
Timbal (II) |
|
29. |
Pb4+ |
Timbal (IV) |
|
30. |
Pt3+ |
Platina (III) |
|
31. |
Cr3+ |
Krom |
|
32. |
NH4+ |
Amonium |
|
33. |
Mn2+ |
Mangan (II) |
|
34. |
Mn3+ |
Mangan (III) |
Daftar Anion
|
No. |
Rumus Anion |
Nama Anion |
|
1. |
Br− |
Bromida |
|
2. |
BrO− |
hipobromit |
|
3. |
BrO3− |
Kalium |
|
4. |
BO33- |
Borat |
|
5. |
Cl− |
Klorida |
|
6. |
ClO− |
Hipoklorit |
|
7. |
ClO2− |
Klorit |
|
8. |
ClO3− |
Klorat |
|
9. |
ClO4− |
Perklorat |
|
10. |
CN− |
Sianida |
|
11. |
CNS− |
Tiosianat |
|
12. |
CH3COO− |
Asetat |
|
13. |
C2O42- |
Oksalat |
|
14. |
CrO42- |
Kromat |
|
15. |
Cr2O72- |
Dikromat |
|
16. |
CO32- |
Karbonat |
|
17. |
F− |
Fluorida |
|
18. |
Fe(CN)64- |
heksasianoferat (II) |
|
19. |
Fe(CN)63- |
heksasianoferat (III) |
|
20. |
H− |
Hidrida |
|
21. |
HSO3− |
Bisulfit |
|
22. |
HSO4− |
Bisulfat |
|
23. |
HCO3− |
Bikarbonat |
|
24. |
S2- |
Sulfida |
|
25. |
SO32- |
Sulfit |
|
26. |
SO42- |
Sulfat |
|
27. |
S2O32- |
Tio sulfat |
|
28. |
NO2− |
Nitrit |
|
29. |
NO3− |
Nitrat |
|
30. |
PO33- |
Fosfit |
|
31. |
PO43- |
Fosfat |
|
32. |
AsO33- |
Arsenit |
|
33. |
AsO33- |
Arsenat |
|
34. |
SiO32- |
Silikat |
|
35. |
AlO33- |
Aluminat |
|
36. |
ZnO22- |
Zinkat |
|
37. |
SnO32- |
Stannat |
|
38. |
I− |
Iodida |
|
39. |
IO− |
Hipoiodit |
|
40. |
IO2− |
Iodit |
|
41. |
IO3− |
Iodat |
|
42. |
IO4− |
Periodat |
|
43. |
N3- |
Nitrida |
|
44. |
O2- |
Oksida |
|
45. |
OH− |
Hidroksida |
Contoh :
- K2SO4 = Kalium sulfat
- (NH4)3PO4 = Amonium fosfat
- (CH3COO)2Pb = Timbal (II) Asetat
- Fe(OH)3 = Besi (III) hidroksida
Tatanama Senyawa Asam & Basa
Tatanama Senyawa Asam
Senyawa asam merupakan senyawa yang dibentuk dari ion hidrogen (H+) dan anion.
Tata Namanya:
Asam + Anion
Contoh :
- H2SO4 = Asam sulfat
- H3PO4 = Asam fosfat
- HClO4 = Asam perklorat
- CH3COOH = Asam asetat
Tatanama Senyawa Basa
Senyawa basa merupakan senyawa yang dibentuk dari kation dan ion hidroksida (OH—).
Tata Namanya:
Kation + Hidroksida
Contoh :
- NaOH = Natrium hidroksida
- Al(OH)3 = Alumunium hidroksida
- Fe(OH)2 = Besi (II) hidroksida
- NH4OH = Amonium hidroksida
Soal Essai
Soal No.1
Tuliskan nama senyawa berikut ini:
- PbO2
- CuI2
- Fe2(CO3)3
- Sn(SO4)2
- MnCl2
PEMBAHASAN :
- Timbal(IV) Oksida
- Tembaga(II) Iodida
- Besi(III) Karbonat
- Timah(II) Sulfat
- Mangan(II) Klorida
Soal No.2
Tuliskan rumus kimia dari senyawa berikut:
- tembaga (II) sulfida
- emas(III) klorida
- timbal(II) nitrat
- titanium(IV) oksida
- vanadium(V) klorida
PEMBAHASAN :
- CuS
- AuCl3
- Pb(NO3)2
- TiO2
- VCl5
Soal No.3
Tuliskan nama senyawa berikut:
a. P2O5
b. Na2O
c. CuBr2
d. (NH4)2SO4
PEMBAHASAN :
- P2O5 termasuk senyawa kovalen karena tersusun dari non logam dan non logam, maka dalam tata nama harus menyebutkan jumlah atomnya. Sehingga namanya adalah Diposfor pentaoksida
- Na2O termasuk senyawa ion karena tersusun dari logam dan non logam. Logamnya hanya memiliki 1 biloks sehingga tidak perlu disebutkan biloksnya. Penamaannya tanpa perlu menyebut jumlah atomnya. Sehingga namanya menjadi Natrium oksida
- CuBr2 termasuk senyawa ion karena tersusun dari logam dan non logam. Logamnya memiliki lebih dari 1 biloks sehingga perlu disebutkan biloksnya dalam bentuk angka romawi. Biloks dari Cu dalam senyawa CuBr2 adalah +2. Penamaannya tanpa perlu menyebut jumlah atomnya. Sehingga namanya menjadi Tembaga (II) bromida
- (NH4)2SO4 disebut juga senyawa poliatomik karena tersusun dari beberapa atom. Senyawa tersebut tersusun dari ion NH4+ yang memiliki nama ion amonium dan ion SO42- yang memiliki nama sulfat. Jadi namanya cukup menggabungkan nama kation dan anionnya yaitu amonium sulfat
Soal No.4
Apa perbedaan antara rumus kimia, rumus molekul, dan rumus empiris?
PEMBAHASAN :
Rumus kimia menyatakan komposisi dari partikel terkecil penyusun zat, dinyatakan dengan angka. rumus molekul menyatakan jenis dan jumlah sesungguhnya dari atom-atom yang menyusun suatu molekul, yang dinyatakan dengan lambang unsur-unsurnya. Rumus empiris menunjukkan jenis dan perbandingan paling sederhana dari atom-atom penyusun suatu zat
Soal No.5
Bagaimana rumus empiris dari senyawa-senyawa berikut:
- C2H4
- C6H6
- P4H10
- Al2Br6
- K2Cr2O7
PEMBAHASAN :
Rumus empiris adalah rumus yang paling sederhana. Senyawa pada soal merupakan rumus molekul yaitu rumus sebenarnya. Untuk mendapatkan rumus empiris, rumus molekul dapat disederhanakan perbandingannya. Sehingga rumus empirisnya adalah:
- CH2
- CH
- P2O5
- Al2Br3
- K2Cr2O7
Soal No.6
Apa perbedaan dari rumus kimia P4 dan 4P?
PEMBAHASAN :
P4 : satu molekul posfor (gabungan dari 4 atom posfor)
4P : empat atom posfor
Soal No.7
Asam cuka dan glukosa mempunyai rumus empiris yang sama, yatu CH2O. Perbedaan terdapat pada jumlah atomnya, di mana untuk asam cuka kelipatan 2 sedangkan glukosa kelipatan 6. Tuliskan rumus molekul asam cuka dan glukosa tersebut.
PEMBAHASAN :
Rumus Molekul asam cuka : (CH2O)2 = C2H4O2 =CH3COOH
Rumus Molekul glukosa : (CH2O)6 = C6H12O6
Soal No.8
Tuliskan rumus kimia senyawa ion yang terbentuk dari gabungan ion Al3+ dengan ion SO42- dan antara ion NH4+ dengan ion CrO42-
PEMBAHASAN :
Al3+ + SO42- → Al2(SO4)3
NH4+ + CrO42- → (NH4)2CrO4
Soal No.9
Setiap molekul gula tersusun 12 buah atom karbon, 22 atom hidrogen dan 11 buah atom oksigen. Tuliskan rumus molekul dan rumus empiris dari molekul gula tersebut.
PEMBAHASAN :
Rumus Molekul gula : C12H22O11
Rumus empiris gula : C12H22O11
Soal No.10
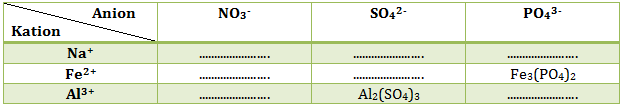
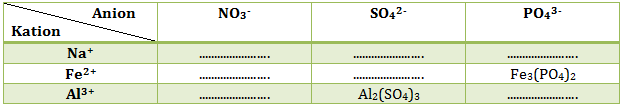
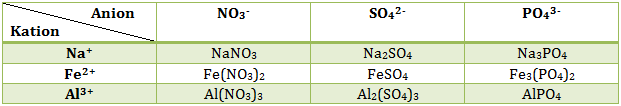
Lengkapi tabel berikut:
Soal No.11
Sebutkan nama dari senyawa berikut:
- MgS e. Na2SO4 i. FeCl3
- NH4OH f. SiO2 j. CuSO4
- P2O5 g. Cl2O k. CaCO3
- Cr2O3 h. Mg3N2 l. ZnCl2
PEMBAHASAN :
- Magnesium sulfida e. Natrium sulfat i. Besi (III) klorida
- Amonium hidroksida f. Silikon dioksida j. Tembaga (II) Sulfat
- Diposfor pentaoksida g. diklor monoksida k. Kalsium karbonat
- Krom (III) oksida h. Magnesium nitrida l. Zink klorida
Soal No.12
Tuliskan rumus kimia dari senyawa-senyawa berikut:
- silikon tetrafluorida
- kobalt(III) nitrat
- karbon disulfida
- besi(II) fosfat
- alumunium silikat
- kalium nitrat
- dinitrogen monoksida
- kalium dikromat
PEMBAHASAN :
- SiF4 d. Fe3(PO4)2 g. N2O
- Co(NO3)3 e. Al2(SiO3)3 h. K2Cr2O7
- CS2 f. KNO3
Soal Pilihan Ganda
Soal No.13
Magnesium Sulfat ditunjukkan oleh rumus kimia….
- KMnO4
- Ni(NO3)2
- MgSO4
- CaCO3
- BaCl2
PEMBAHASAN :
Magnesium sulfat terdiri dari ion Mg2+ dan ion sulfat SO42-. perbandingan muatan (+) dan (-) nya = 1 : 1, sehingga akan membentuk senyawa MgSO4. Opsi jawaban lainnya.
- KMnO4 = Kalium permanganat
- Ni(NO3)2 = Nikel Nitrat
- CaCO3 = Kalsium karbonat
- BaCl2 = Barium klorida
Jawaban C
Soal No.14
Nama senyawa PbCl2 adalah….
- Timbal klorida
- Timbal (II) klorida
- Timbal (III) klorida
- Timbal (IV) klorida
- Timbal diklorida
PEMBAHASAN :
Timbal termasuk kedalam logam yang memiliki biloks lebih dari satu yaitu +2 dan +4 dari perhitungan biloks Pb, biloksnya = +2, sehingga namanya adalah Timbal (II) klorida.
Jawaban B
Soal No.15 (UN 2005)
Nama yang tepat untuk senyawa Fe2O, adalah….
- Besi (I) oksida
- Besi (II) oksida
- Besi (III) oksida
- Besi (II) sulfida
- Besi sulfida
PEMBAHASAN :
Menghitung biloks Fe dari senyawa Fe2O
B.o Fe x 2 + B.o O x 1 = 0
2 B.o Fe + (-2) = 0
B.o Fe = +1
Maka namanya adalah Besi (I) oksida
Jawaban A
Gimana belajar tata nama senyawa binernya, kalau ada yang kurang paham bisa kamu tanya di kolom komentar yah. Ok demikian rangkuman materi dan contoh soal tata nama senyawa biner berikut video pembelajarannya. Semoga berguna buat kalian. Kalau bermanfaat bantu kita juga yah untuk share dan beritahu teman kamu untuk berkunjung kesini. Terima kasih.
Semoga Bermanfaat