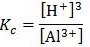pembahasan selanjutnya adalah
- tetapan kesetimbangan kimia,
- polimer,
- penerapan sifat koligatif larutan,
- sifat koligatif larutan, serta
- reaksi reduksi dan oksidasi.
Soal No. 26 tentang Tetapan Kesetimbangan Kimia
Tetapan kesetimbangan (Kc) suatu reaksi adalah sebagai berikut:
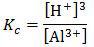
Persamaan reaksi kesetimbangan yang sesuai adalah ….
A. Al(OH)3(s) + 3H+(aq) ⇌ Al3+(aq) + 3H2O(l)
B. Al3+(aq) + 3H2O(l) ⇌ Al(OH)3(s) + 3H+(aq)
C. Al(OH)3(aq) + 3H+(aq) ⇌ Al3+(aq) + 3H2O(l)
D. Al3+(aq) + 3H2O(l) ⇌ Al(OH)3(aq) + 3H+(aq)
E. Al(OH)3(s) + 6H+(aq) ⇌ Al3+(aq) + 3H2O(l)
Pembahasan
Konstanta kesetimbangan konsentrasi (Kc) adalah perbandingan konsentrasi hasil reaksi terhadap konsentrasi pereaksi pangkat koefisien masing-masing dengan syarat masing-masing spesi kimia tersebut harus dalam wujud gas (g) atau larutan (aq).
Sesuai dengan tetapan kesetimbangan yang diketahui pada soal, persamaan reaksi yang sesuai adalah
Al3+(aq) + 3H2O(l) ⇌ Al(OH)3(s) + 3H+(aq)
Jadi, persamaan reaksi kesetimbangan yang sesuai adalah opsi (B).
Perdalam materi ini di Pembahasan Kimia UN: Kesetimbangan Reaksi.
Soal No. 27 tentang Polimer

Polimer yang dihasilkan serta kegunaannya yang paling tepat berikut ini adalah ….
| Polimer | Kegunaan | |
| A. | nilon 66 | serat kain |
| B. | PVC | pipa/talang air |
| C. | teflon | panci antilengket |
| D. | kevlar | rompi antipeluru |
| E. | polipropilena | botol plastik |

Pembahasan
Monomer pada soal di atas adalah kloroetena atau vinil klorida. Monomer ini akan membentuk polimer poli vinil klorida (PVC). Di antara kegunaannya adalah untuk pipa paralon.
Berikut ini polimer, monomer, dan kegunaannya pada soal di atas.
| Polimer | Monomer | Kegunaan |
| nilon 66 | asam adipat + 1,6-diaminoheksana | serat kain |
| PVC | CH2=CHCl (vinil klorida) | pipa/talang air |
| teflon | CF2=CF2 (tetrafluoro etena) | panci antilengket |
| kevlar | 1,4-asam dikarboksilat benzena + 1,4 diamino benzena | rompi antipeluru |
| polipropilena | CH2=CH−CH3 (propena/propilena) | botol plastik |
Jadi, pasangan polimer dan kegunaannya yang paling tepat adalah opsi (B).
Perdalam materi ini di Pembahasan Kimia UN: Polimer.
Soal No. 28 tentang Penerapan Sifat Koligatif Larutan
- penyerapan air oleh akar tanaman,
- penambahan garam dalam es putar,
- penambahan garam untuk mencairkan salju,
- penggunaan garam untuk membunuh lintah, dan
- menambahkan etilen glikol pada radiator mobil.
Penerapan tekanan osmotik terdapat pada peristiwa nomor ….
A. (1) dan (3)
B. (1) dan (4)
C. (2) dan (3)
D. (2) dan (5)
E. (4) dan (5)
Pembahasan
Penjelasan tentang penerapan sifat koligatif larutan yang disebutkan pada soal adalah sebagai berikut.
- Akar tanaman mengandung zat-zat terlarut dengan konsentrasi lebih tinggi sehingga mempunyai tekanan osmotik yang lebih tinggi pula daripada air di sekelilingnya, akibatnya air terserap ke dalam akar tanaman. [tekanan osmotik]
- Penambahan garam pada kepingan es batu akan menurunkan titik beku es sehingga es mencair. Es cair ini digunakan sebagai cairan pendingin pada pembuatan es putar. [penurunan titik beku]
- Penambahan garam akan menurunkan titik beku salju sehingga salju mencair. [penurunan titik beku]
- Penggunaan garam pada tubuh lintah menyebabkan cairan tubuh lintah keluar karena tekanan osmotik garam lebih tinggi. Akibatnya lintah mati karena kekurangan cairan. [tekanan osmotik]
- Penambahan etilen glikol pada radiator mobil akan menurunkan titik beku air radiator sehingga air radiator tetap cair dan tidak mudah membeku. [penurunan titik beku]
Jadi, penerapan tekanan osmotik terdapat pada peristiwa nomor 1 dan 4 (B).
Soal No. 29 tentang Sifat Koligatif Larutan

Larutan yang mempunyai tekanan uap paling kecil ditunjukkan oleh gambar nomor ….
A. (1)
B. (2)
C. (3)
D. (4)
E. (5)
Pembahasan
Perhatikan rumus tekanan uap larutan berikut ini!
p = po.xp
Berdasarkan rumus di atas, tekanan uap larutan (p) berbanding lurus dengan fraksi mol pelarut (xp). Sedangkan fraksi adalah salah satu besaran konsentrasi (banyaknya partikel).
Dengan demikian, larutan yang mempunyai tekanan uap kecil adalah larutan yang mempunyai fraksi mol pelarut atau zat pelarut (bulatan putih) yang paling sedikit.
Jadi, larutan yang mempunyai tekanan uap paling kecil ditunjukkan oleh gambar nomor (5).
Perdalam soal no. 28 dan 29 di Pembahasan Kimia UN: Sifat Koligatif Larutan.
Soal No. 30 tentang Reaksi Reduksi dan Oksidasi
2MnO2(s) + 2NH4+(aq) + Zn(s) → Mn2O3(s) + Zn2+(aq) + 2NH3(aq) + 2H2O(l)
Spesi kimia yang bertindak sebagai reduktor dan hasil reduksinya adalah ….
A. MnO2(s) dan Mn2O3(s)
B. NH4+(aq) dan NH3(aq)
C. Zn(s) dan Mn2O3(s)
D. NH4+(aq) dan H2O(l)
E. MnO2(aq) dan NH4+(aq)
Pembahasan
Kita tentukan dulu bilangan oksidasi dan perubahannya tiap unsur yang terlibat dalam reaksi di atas selain unsur H dan O. Keberadaan koefisien dan fase zat tidak perlu diperhitungkan.
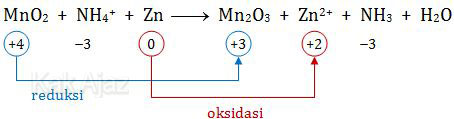
Perhatikan gambar di atas!
- MnO2 mengalami reduksi menjadi Mn2O3, berarti:
MnO2 : oksidator
Mn2O3 : hasil reduksi
- Zn mengalami oksidasi menjadi Zn2+, berarti:
Zn : reduktor
Zn2+ : hasil oksidasi
Jadi, Spesi kimia yang bertindak sebagai reduktor adalah Zn dan hasil reduksinya Mn2O3 adalah (C).
Perdalam materi ini di Pembahasan Kimia UN: Reaksi Redoks dan Elektrokimia.
Simak Pembahasan Soal Kimia UN 2016 selengkapnya.
Dapatkan pembahasan soal dalam file pdf di sini.
Terimakasih
Semoga Bermanfaat