Untuk Pembelajaran selanjutnya…
Soal No.1
Zat di bawah ini yang termasuk elektrolit senyawa kovalen dan bersifat asam adalah….
- NaOH
- NaCl
- C12H22O11
- HBr
- CH3OH
PEMBAHASAN :
Senyawa kovalen tersusun dari non logam dan non logam, sedangkan zat yang bersifat asam akan melepaskan ion H+ jika dilarutkan dalam air (memiliki atom H). Penjelasan tiap opsi sebagai berikut:
- NaOH : Elektrolit yang berikatan ionik & kovalen dan bersifat basa
- NaCl : Elektrolit yang berikatan ionik dan bersifat netral
- C12H22O11 : Non elektrolit
- HBr : Elektrolit yang berikatan kovalen dan bersifat asam.
- CH3OH : Non elektrolit
Sehingga jawaban yang benar adalah D
Jawaban D
Soal No.2
Di bawah ini, yang dapat menghantarkan listrik paling baik adalah….
- Larutan C6H12O6
- Larutan H2SO4
- Larutan H3PO4
- Larutan Be(OH)2
- Larutan CO(NH2)2
PEMBAHASAN :
- Larutan C6H12O6 : Non elektrolit
- Larutan H2SO4 : Elektrolit kuat
- Larutan H3PO4 : Elektrolit lemah
- Larutan Be(OH)2 : Elektrolit lemah
- Larutan CO(NH2)2 : Non elektrolit
Maka larutan yang dapat menghantarkan listrik paling baik adalah larutan elektrolit kuat yaitu H2SO4
Jawaban B
Soal No.3
Spesi kimia yang menghantarkan listrik di dalam larutan KSCN adalah ….
- ion-ion S2– dan KCN2+
- ion-ion KS+ dan CN–
- ion-ion K+ dan SCN–
- molekul KSCN dan H2O
- ion-ion K+ dan H2O
PEMBAHASAN :
larutan KSCN merupakan larutan elektrolit yang akan mengalami ionisasi dalam air menjadi ion K+ dan ion SCN–. Ion-ion ini yang menyebabkan larutan KSCN dapat menghantarkan listrik
Jawaban C
Soal No.4
Ke dalam air ditambahkan cuka (CH3COOH) dan alkohol (C2H5OH) kemudian diuji sifat listriknya. Spesi kimia yang menghantarkan arus listrik adalah ….
- C2H5OH
- CH3COO– dan H+
- H2O
- C2H5OH dan H2O
- CH3COOH
PEMBAHASAN :
CH3COOH termasuk zat yang dapat menghantarkan listrik jika dilarutkan ke dalam air menghasilkan ion CH3COO– dan H+. Sedangkan C2H5OH tidak dapat menghantarkan listrik atau non elektrolit. Maka spesi yang dapat menghantarkan listrik adalah CH3COO– dan H+
Jawaban B
Soal No.5
Di antara campuran berikut, ketika dalam air membentuk larutan nonelektrolit adalah ….
- CH3COOH + NaCl
- C2H5OH + C12H22O11
- Spiritus + HCl
- C2H5OH + NaCl
- C12H22O11 + CH3COOH
PEMBAHASAN :
- CH3COOH + NaCl = Elektrolit lemah dan elektrolit kuat
- C2H5OH + C12H22O11 = Non elektrolit dan non elektrolit
- Spiritus + HCl = Non elektrolit dan elektrolit kuat
- C2H5OH + NaCl = Non elektrolit dan elektrolit kuat
- C12H22O11 + CH3COOH = Non elektrolit dan elektrolit lemah
Jawaban B
Soal No.6
Bilangan oksidasi atom C yang diberi bintang (*) adalah….
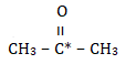
- -2
- -1
- +1
- +2
PEMBAHASAN :
Pada penentuan bilangan oksidasi senyawa organik. Alkil akan memiliki biloks = 0. Karena biloks O = -2. Maka biloks C yang ditandai adalah +2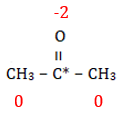
Jawaban E
Soal No.7
Bilangan oksidasi fosfor paling rendah terdapat pada senyawa…
- PH4Br
- POBr3
- PF3
- PCl5
- Ca3(PO4)2
PEMBAHASAN :
- PH4Br
Biloks P x 1 + biloks H x 4 + biloks Br x 1 = 0
Biloks P + 1 x 4 + (-1) x 1 = 0
Biloks P + 3 = 0
Biloks P = -3 - POBr3
Biloks P x 1 + biloks O x 1 + biloks Br x 3 = 0
Biloks P + (-2) x 1 + (-1) x 3 = 0
Biloks P + (-5) = 0
Biloks P = +5 - PF3
Biloks P x 1 + biloks F x 3 = 0
Biloks P + (-1) x 3 = 0
Biloks P – 3 = 0
Biloks P = +3 - PCl5
Biloks P x 1 + biloks Cl x 5 = 0
Biloks P + (-1) x 5 = 0
Biloks P – 5 = 0
Biloks P = +5 - Ca3(PO4)2
Biloks Ca x 3 + biloks P x 2 + biloks O x 8 = 0
+2 x 3 + 2xBiloks P + (-2) x 8 = 0
2xBiloks P + (-10) = 0
Biloks P = +5
Maka biloks fosfor yang paling rendah adalah PH4Br yaitu -3
Jawaban A
Soal No.8
Reaksi berikut yang bukan merupakan reaksi redoks adalah …
- (NH4)2Cr2O7(aq) → N2(g) + 4H2O(l) + Cr2O3(s)
- CuCO3(s) + H2SO4(aq) → CuSO4(s) + H2O(l) + CO2(g)
- H2S(g)+ 2H2O(l) + 3Cl2(g) → SO2(g) + 6HCl(aq)
- Mg(s) + CuSO4(s) → MgSO4(s) + Cu(s)
- 3CH3CHOHCH3(aq)+ 2Cr2O3 (s) → 3CH3COCH3(aq) + 2Cr(OH)3(s)
PEMBAHASAN :
Cara cepat menentukan suatu reaksi merupakan redoks atau bukan yaitu jika ada unsur bebas (molekul unsur atau unsur) maka termasuk reaksi redoks. Cara biasa yaitu dengan menghitung satu-satu biloksnya dimana reaksi redoks terdapat zat yang naik dan turun biloksnya.
- (NH4)2Cr2O7(aq) → N2(g) + 4H2O(l) + Cr2O3(s)
Terdapat unsur bebas sehingga bisa merupakan reaksi redoks - CuCO3(s) + H2SO4(aq) → CuSO4(s) + H2O(l) + CO2(g)
Bukan merupakan reaksi redoks karena tidak ada zat yang berubah biloksnya - H2S(g)+ 2H2O(l) + 3Cl2(g) → SO2(g) + 6HCl(aq)
Terdapat unsur bebas sehingga bisa merupakan reaksi redoks - Mg(s) + CuSO4(s) → MgSO4(s) + Cu(s)
Terdapat unsur bebas sehingga bisa merupakan reaksi redoks - 3CH3CHOHCH3(aq)+ 2CrO3 (s) → 3CH3COCH3(aq) + 2Cr(OH)3(s)
Tidak terdapat unsur bebas namun terjadi kenaikan biloks dari unsur C dari 0 ke +2 dan terjadi penurunan biloks dari unsur Cr dari +6 menjadi +3
Jawaban B
Soal No.9
Pada reaksi: FeI2(aq) + Cl2(g) → FeCl2(aq) + I2(s) molekul klorin ….
- mengoksidasi ion I–
- mengoksidasi ion Fe2+
- mereduksi ion I–
- mereduksi ion Fe2+
- berperan sebagai reduktor
PEMBAHASAN :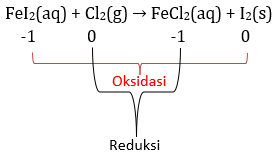
Klorin (Cl2) mengalami reduksi atau mengoksidasi ion I– menjadi I2
Jawaban A
Soal No.10
Natrium perborat (Na2B4O7) merupakan obat kumur yang disarankan. Pembuatannya menurut reaksi berikut.
Na2B4O7(aq) + Na2O2(aq) + H2O2(aq) → 4NaBO3(aq) + 3H2O(l)
Fungsi natrium perborat dalam obat kumur adalah….
- bersifat sebagai pembunuh kuman
- bersifat oksidator
- bersifat reduktor
- sebagai emulgator
- sebagai flokulan
PEMBAHASAN :
Natrium perborat (Na2B4O7) mengalami oksidasi sehingga dikatakan bersifat reduktor
Jawaban C
Soal No.11
Fe2O3 adalah rumus kimia untuk senyawa . . . .
- besi oksida
- dibesi trioksida
- besi(II) oksida
- besi(II) besi(III) oksida
- besi(III) oksida
PEMBAHASAN :
Fe2O3 terdiri dari unsur Fe yaitu logam yang memiliki biloks lebih dari satu jenis (ditulis biloksnya) dan O yaitu non logam. Maka termasuk ke dalam senyawa ion dimana penamaannya tidak menyebutkan jumlah atomnya. Biloks Fe dalam senyawa tersebut adalah +3 sehingga tata namanya adalah besi (III) oksida
Jawaban E
Soal No.12
Diberikan beberapa kation dan anion sebagai berikut: CNS– ; Cr3+; SiO32- ; SbO43- ; Cd2+; dan NH4+. Rumus kimia dan nama senyawa yang benar dari ion-ion tersebut adalah…
- Cd(CNS)2: kadmium sianat
- Cr2(SiO3)3; krom (III) silikat
- (NH4)3(SbO4)4; amonium antimonat
- CdSbO4; kadmium antimonat
- NH4CNS ; amonium sianida
PEMBAHASAN :
Maka jawaban yang benar adalah B
Jawaban B
Soal No.13
Di antara persamaan molekuler berikut, reaksi yang sudah setara adalah ….
- 2CuO(s) + 2C(s) ⎯⎯→ Cu(s) + 4CO2(g)
- SO2(g) + 2O2(g) ⎯⎯→ SO3(g)
- H2S(g) + O2(g) ⎯⎯→ H2O(l) + SO2(g)
- C(s) + O2(g) ⎯⎯→ CO(g)
- 2NO(g) + O2(g) ⎯⎯→ 2NO2(g)
PEMBAHASAN :
Penjelasan tiap pilihan jawaban
- Cu, C dan O belum setara
- O belum setara
- O belum setara
- O belum setara
- Reaksi sudah setara
Maka jawaban yang benar adalah E
Jawaban E
Soal No.14
Pembakaran sempurna gas etana menghasilkan CO2 dan H2O seperti ditunjukkan pada persamaan reaksi berikut. C2H6(g) + O2(g) ⎯⎯→ CO2(g) + H2O(l) Pada persamaan ini, perbandingan koefisien reaksi CO2 terhadap H2O adalah ….
- 1 : 1
- 1 : 3
- 2 : 3
- 3 : 1
- 3 : 2
PEMBAHASAN :
Maka perbandingan koefisien reaksi CO2 terhadap H2O adalah 2 : 3
Jawaban C
Soal No.15
Perhatikan persamaan reaksi setara berikut. X + Pb(NO3)2(aq) ⎯⎯→ PbCl2(s) + NaNO3(aq) Senyawa X adalah ….
- HNO3
- HCl
- NaNO3
- NaCl2
- NaCl
PEMBAHASAN :
Pada reaksi tersebut di ruas kanan terdapat atom Na dan atom Cl yang tidak ada di ruas kiri. Maka Senyawa X tersebut mengandung unsur Na dan Cl yang terdapat diruas kanan. Sehingga senyawa tersebut adalah NaCl
Jawaban E
Semoga Bermanfaat